| PSMA3 |
|---|
 |
| Наявні структури |
|---|
| PDB | Пошук ортологів: PDBe RCSB |
|---|
| Список кодів PDB | | 4R3O, 4R67, 5DSV, 5A0Q | | |
| Ідентифікатори |
|---|
| Символи | PSMA3, HC8, PSC3, proteasome subunit alpha 3, proteasome 20S subunit alpha 3 |
|---|
| Зовнішні ІД | OMIM: 176843 MGI: 104883 HomoloGene: 2082 GeneCards: PSMA3 |
|---|
| |
| Реагує на сполуку |
|---|
| Карфілзоміб, ixazomib, Oprozomib[1] |
| Онтологія гена |
|---|
| Молекулярна функція | • endopeptidase activity
• GO:0070122 peptidase activity
• GO:0001948, GO:0016582 protein binding
• threonine-type endopeptidase activity
• hydrolase activity
• ubiquitin protein ligase binding
|
|---|
| Клітинна компонента | • цитоплазма
• гіалоплазма
• нуклеоплазма
• Протеасома
• екзосома
• клітинне ядро
• proteasome core complex
• синапс
• proteasome core complex, alpha-subunit complex
|
|---|
| Біологічний процес | • regulation of cellular amino acid metabolic process
• antigen processing and presentation of exogenous peptide antigen via MHC class I, TAP-dependent
• regulation of mRNA stability
• ubiquitin-dependent protein catabolic process
• positive regulation of canonical Wnt signaling pathway
• protein polyubiquitination
• stimulatory C-type lectin receptor signaling pathway
• tumor necrosis factor-mediated signaling pathway
• протеоліз
• MAPK cascade
• Fc-epsilon receptor signaling pathway
• NIK/NF-kappaB signaling
• anaphase-promoting complex-dependent catabolic process
• proteolysis involved in cellular protein catabolic process
• T cell receptor signaling pathway
• negative regulation of canonical Wnt signaling pathway
• regulation of endopeptidase activity
• GO:0022415 viral process
• Wnt signaling pathway, planar cell polarity pathway
• proteasome-mediated ubiquitin-dependent protein catabolic process
• negative regulation of G2/M transition of mitotic cell cycle
• protein deubiquitination
• SCF-dependent proteasomal ubiquitin-dependent protein catabolic process
• трансмембранний транспорт
• regulation of transcription from RNA polymerase II promoter in response to hypoxia
• посттрансляційна модифікація
• regulation of hematopoietic stem cell differentiation
• proteasomal protein catabolic process
• proteasomal ubiquitin-independent protein catabolic process
• interleukin-1-mediated signaling pathway
• regulation of mitotic cell cycle phase transition
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
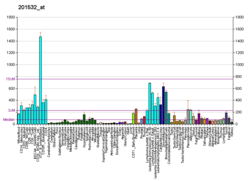 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | | NM_011184
NM_001310595
NM_001310596 |
|
|---|
| RefSeq (білок) | | | NP_001297524
NP_001297525
NP_035314 |
|
|---|
| Локус (UCSC) | Хр. 14: 58.24 – 58.27 Mb | Хр. 12: 71.02 – 71.04 Mb |
|---|
| PubMed search | [2] | [3] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
PSMA3 (англ. Proteasome subunit alpha 3) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 14-ї хромосоми.[4] Довжина поліпептидного ланцюга білка становить 255 амінокислот, а молекулярна маса — 28 433[5].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MSSIGTGYDL | | SASTFSPDGR | | VFQVEYAMKA | | VENSSTAIGI | | RCKDGVVFGV |
| EKLVLSKLYE | | EGSNKRLFNV | | DRHVGMAVAG | | LLADARSLAD | | IAREEASNFR |
| SNFGYNIPLK | | HLADRVAMYV | | HAYTLYSAVR | | PFGCSFMLGS | | YSVNDGAQLY |
| MIDPSGVSYG | | YWGCAIGKAR | | QAAKTEIEKL | | QMKEMTCRDI | | VKEVAKIIYI |
| VHDEVKDKAF | | ELELSWVGEL | | TNGRHEIVPK | | DIREEAEKYA | | KESLKEEDES |
| DDDNM |
Кодований геном білок за функціями належить до гідролаз, протеаз, треонінових протеаз. Задіяний у такому біологічному процесі як взаємодія хазяїн-вірус. Локалізований у цитоплазмі, ядрі.
Література
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Kristensen P., Johnsen A.H., Uerkvitz W., Tanaka K., Hendil K.B. (1994). Human proteasome subunits from 2-dimensional gels identified by partial sequencing. Biochem. Biophys. Res. Commun. 205: 1785—1789. PMID 7811265 DOI:10.1006/bbrc.1994.2876
- Claverol S., Burlet-Schiltz O., Girbal-Neuhauser E., Gairin J.E., Monsarrat B. (2002). Mapping and structural dissection of human 20 s proteasome using proteomic approaches. Mol. Cell. Proteomics. 1: 567—578. PMID 12376572 DOI:10.1074/mcp.M200030-MCP200
- Yano M., Koumoto Y., Kanesaki Y., Wu X., Kido H. (2004). 20S proteasome prevents aggregation of heat-denatured proteins without PA700 regulatory subcomplex like a molecular chaperone. Biomacromolecules. 5: 1465—1469. PMID 15244466 DOI:10.1021/bm049957a
- Westhoff B., Chapple J.P., van der Spuy J., Hoehfeld J., Cheetham M.E. (2005). HSJ1 is a neuronal shuttling factor for the sorting of chaperone clients to the proteasome. Curr. Biol. 15: 1058—1064. PMID 15936278 DOI:10.1016/j.cub.2005.04.058
- Touitou R., O'Nions J., Heaney J., Allday M.J. (2005). Epstein-Barr virus EBNA3 proteins bind to the C8/alpha7 subunit of the 20S proteasome and are degraded by 20S proteasomes in vitro, but are very stable in latently infected B cells. J. Gen. Virol. 86: 1269—1277. PMID 15831937 DOI:10.1099/vir.0.80763-0
Примітки
- ↑ Сполуки, які фізично взаємодіють з Proteasome 20S subunit alpha 3 переглянути/редагувати посилання на ВікіДаних.
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:9532 (англ.) . Архів оригіналу за 23 вересня 2017. Процитовано 21 серпня 2017.
- ↑ UniProt, P25788 (англ.) . Архів оригіналу за 19 вересня 2017. Процитовано 21 серпня 2017.
Див. також
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|
| На цю статтю не посилаються інші статті Вікіпедії. Будь ласка розставте посилання відповідно до прийнятих рекомендацій. |
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |











