| HSPA4 |
|---|
|
| Ідентифікатори |
|---|
| Символи | HSPA4, APG-2, HEL-S-5a, HS24/P52, HSPH2, RY, hsp70, hsp70RY, heat shock protein family A (Hsp70) member 4 |
|---|
| Зовнішні ІД | OMIM: 601113 MGI: 1342292 HomoloGene: 1624 GeneCards: HSPA4 |
|---|
| Онтологія гена |
|---|
| Молекулярна функція | • nucleotide binding
• GO:0001948, GO:0016582 protein binding
• ATP binding
|
|---|
| Клітинна компонента | • цитоплазма
• гіалоплазма
• екзосома
• клітинне ядро
|
|---|
| Біологічний процес | • response to unfolded protein
• protein insertion into mitochondrial outer membrane
• chaperone-mediated protein complex assembly
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
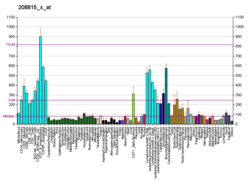
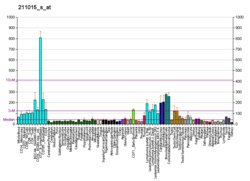
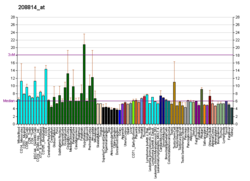 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | |
|---|
| RefSeq (білок) | | |
|---|
| Локус (UCSC) | Хр. 5: 133.05 – 133.11 Mb | Хр. 11: 53.15 – 53.19 Mb |
|---|
| PubMed search | [1] | [2] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
HSPA4 (англ. Heat shock protein family A (Hsp70) member 4) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 5-ї хромосоми. [3] Довжина поліпептидного ланцюга білка становить 840 амінокислот, а молекулярна маса — 94 331[4].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MSVVGIDLGF | | QSCYVAVARA | | GGIETIANEY | | SDRCTPACIS | | FGPKNRSIGA |
| AAKSQVISNA | | KNTVQGFKRF | | HGRAFSDPFV | | EAEKSNLAYD | | IVQLPTGLTG |
| IKVTYMEEER | | NFTTEQVTAM | | LLSKLKETAE | | SVLKKPVVDC | | VVSVPCFYTD |
| AERRSVMDAT | | QIAGLNCLRL | | MNETTAVALA | | YGIYKQDLPA | | LEEKPRNVVF |
| VDMGHSAYQV | | SVCAFNRGKL | | KVLATAFDTT | | LGGRKFDEVL | | VNHFCEEFGK |
| KYKLDIKSKI | | RALLRLSQEC | | EKLKKLMSAN | | ASDLPLSIEC | | FMNDVDVSGT |
| MNRGKFLEMC | | NDLLARVEPP | | LRSVLEQTKL | | KKEDIYAVEI | | VGGATRIPAV |
| KEKISKFFGK | | ELSTTLNADE | | AVTRGCALQC | | AILSPAFKVR | | EFSITDVVPY |
| PISLRWNSPA | | EEGSSDCEVF | | SKNHAAPFSK | | VLTFYRKEPF | | TLEAYYSSPQ |
| DLPYPDPAIA | | QFSVQKVTPQ | | SDGSSSKVKV | | KVRVNVHGIF | | SVSSASLVEV |
| HKSEENEEPM | | ETDQNAKEEE | | KMQVDQEEPH | | VEEQQQQTPA | | ENKAESEEME |
| TSQAGSKDKK | | MDQPPQAKKA | | KVKTSTVDLP | | IENQLLWQID | | REMLNLYIEN |
| EGKMIMQDKL | | EKERNDAKNA | | VEEYVYEMRD | | KLSGEYEKFV | | SEDDRNSFTL |
| KLEDTENWLY | | EDGEDQPKQV | | YVDKLAELKN | | LGQPIKIRFQ | | ESEERPKLFE |
| ELGKQIQQYM | | KIISSFKNKE | | DQYDHLDAAD | | MTKVEKSTNE | | AMEWMNNKLN |
| LQNKQSLTMD | | PVVKSKEIEA | | KIKELTSTCS | | PIISKPKPKV | | EPPKEEQKNA |
| EQNGPVDGQG | | DNPGPQAAEQ | | GTDTAVPSDS | | DKKLPEMDID |
Задіяний у такому біологічному процесі як відповідь на стрес. Білок має сайт для зв'язування з АТФ, нуклеотидами. Локалізований у цитоплазмі.
Література
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Fathallah D.M., Cherif D., Dellagi K., Arnaout M.A. (1993). Molecular cloning of a novel human hsp70 from a B cell line and its assignment to chromosome 5. J. Immunol. 151: 810—813. PMID 8335910
Примітки
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:5237 (англ.) . Архів оригіналу за 14 жовтня 2017. Процитовано 6 лютого 2017.
- ↑ UniProt, P34932 (англ.) . Архів оригіналу за 31 грудня 2016. Процитовано 6 лютого 2017.
Див. також
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|













 HSPA4
HSPA4