
Nutrição pré-natal aborda as recomendações de nutrientes antes e durante a gravidez. A nutrição e o controle de peso antes e durante a gravidez têm um efeito profundo no desenvolvimento dos bebês. Este é um período crítico para o desenvolvimento saudável, já que os bebês dependem fortemente dos estoques e nutrientes maternos para um crescimento ideal e para resultados de saúde ao longo da vida.[1]
A nutrição pré-natal tem forte influência sobre o peso ao nascer e no desenvolvimento posterior do bebê. Um estudo do Instituto Nacional de Saúde dos Estados Unidos (NIH) descobriu que bebês nascidos de mães obesas têm maior probabilidade de falhar em testes de habilidades motoras finas, que envolvem o movimento de pequenos músculos, como mãos e dedos.[2]
Um ditado comum de que a mulher "está comendo por dois" durante a gravidez implica que a mãe deve consumir o dobro de alimentos nesse período, mas isso é enganoso. Embora o consumo materno afete diretamente tanto a mãe quanto o feto em crescimento, comer em excesso comprometerá a saúde do bebê, que terá de se esforçar mais para ser saudável no futuro. Em comparação com o bebê, a mãe apresenta menor risco biológico. Portanto, o excesso de calorias, em vez de ir para o bebê, frequentemente é armazenado como gordura na mãe.[3] Por outro lado, o consumo insuficiente resultará em menor peso ao nascer.
Manter um peso saudável durante a gestação reduz riscos adversos para os bebês, como defeitos congênitos, bem como condições crônicas na vida adulta, como obesidade, diabetes e doença cardiovascular (DCV).[4] Idealmente, a taxa de ganho de peso deve ser monitorada durante a gravidez para apoiar o desenvolvimento mais adequado do bebê.[5]
Contexto
[editar | editar código fonte]Hipótese de Barker: o impacto das condições intrauterinas no crescimento e desenvolvimento fetal
[editar | editar código fonte]A "Hipótese de Barker", ou Fenótipo econômico, afirma que as condições durante a gravidez terão efeitos de longo prazo na saúde adulta. Os riscos associados de doenças ao longo da vida incluem doença cardiovascular, diabetes tipo 2, obesidade e hipertensão. Bebês nascidos com menor peso parecem ter uma taxa maior de mortalidade do que bebês nascidos com peso mais elevado.[6] Isso não significa que bebês com peso elevado sejam menos preocupantes. A taxa de mortalidade aumenta à medida que o peso ao nascer ultrapassa a faixa considerada normal.[7] Portanto, é importante manter um ganho de peso gestacional saudável durante a gravidez para alcançar o peso ideal ao nascer.
Quando essa teoria foi proposta pela primeira vez, não foi bem aceita e foi recebida com muito ceticismo.[8] A principal crítica era que variáveis de fator de confusão — nutrição na infância, taxa de ganho de peso ao longo da infância e outros fatores ambientais — poderiam estar associadas a muitas das condições crônicas observadas nas populações de baixo peso ao nascer. Por isso, havia falta de apoio para que o peso ao nascer fosse reconhecido como fator de risco independente.[7] Pesquisas subsequentes buscaram ajustar esses fatores ambientais e, assim, apresentaram resultados mais convincentes, com variáveis de confusão mínimas.[7]
A "Hipótese de Barker" também é conhecida como "Hipótese da Programação Fetal". A palavra "programação" ilustra a ideia de que, durante períodos críticos do desenvolvimento fetal inicial, ocorrem mudanças persistentes na estrutura e função corporal causadas por estímulos ambientais.[8] Isso se relaciona ao conceito de plasticidade do desenvolvimento, que postula que os genes podem ser expressos em diferentes faixas de estados fisiológicos ou morfológicos em resposta às condições ambientais vivenciadas durante o desenvolvimento fetal.[7] A programação pode ser impactada pela dieta materna, e as implicações dessas mudanças podem persistir por toda a vida da criança.
Estudos em animais mostram que a nutrição materna inadequada pode impactar negativamente a expressão de vários genes, o desenvolvimento de tecidos e órgãos, e pode estar ligada à hipertensão permanente na prole.[8] A nutrição materna vai além da ingestão calórica. Ela abrange uma ampla gama de elementos, como o equilíbrio de macronutrientes incluindo proteínas, carboidratos e ácidos graxos, cada um tendo efeito único no crescimento fetal. Deficiências na dieta da mãe podem enviar sinais ao feto sugerindo que suas condições de vida a longo prazo serão de pobreza.[7] Consequentemente, o bebê adapta-se mudando o tamanho corporal e o metabolismo para se preparar para condições difíceis de escassez de alimentos após o nascimento.[7] Processos fisiológicos e metabólicos no corpo sofrem mudanças permanentes como resultado do crescimento restrito.[7] Quando as condições mudam da desnutrição para a abundância, o bebê é forçado a um ambiente contrário ao que seu corpo foi preparado. Essa discrepância aumenta o risco de desenvolver doenças na vida adulta.[7] Da mesma forma, se o feto em gestação no útero de uma mãe saudável for exposto a fome prolongada após o nascimento, o bebê terá menor capacidade de adaptação ao ambiente hostil do que os bebês de baixo peso ao nascer.[6] Além disso, deficiências de micronutrientes durante a gravidez podem influenciar os resultados de longo prazo relacionados à sobrevivência e ao desenvolvimento cognitivo da prole.[9] Embora essas associações ainda não estejam totalmente estabelecidas, ressaltam a importância da nutrição pré-natal adequada durante esse período crítico.[9]
A importância do ambiente materno em relação ao desenvolvimento fetal tem sido debatida. Estudos mostram que meios-irmãos que compartilham a mesma mãe apresentam pesos ao nascer mais semelhantes do que aqueles que compartilham apenas o pai.[8] Outras pesquisas reforçam essa ideia, sugerindo que mais de 50% das discrepâncias no peso fetal podem ser atribuídas ao ambiente intrauterino, sendo o segundo maior fator os genes maternos.[8] Essa linha de pesquisa dá suporte à hipótese de Barker e destaca a relevância da saúde materna; no entanto, os mecanismos pelos quais esses fatores (como a desnutrição) influenciam o peso fetal ainda estão em investigação.
Hipótese de Pedersen – influências da concentração de glicose materna no crescimento fetal
[editar | editar código fonte]Em 1952, o médico dinamarquês Jørgen Pedersen, da Universidade de Copenhague, formulou a hipótese de que a hiperglicemia materna durante a gestação poderia causar hiperglicemia fetal, expondo assim o feto a níveis elevados de insulina. Isso resultaria em um risco aumentado de macrossomia fetal e hipoglicemia neonatal.[10]
A concentração de glicose no sangue em humanos depende principalmente da dieta, especialmente da ingestão de energia e da porcentagem de carboidratos na alimentação. Altas concentrações de glicose no sangue de gestantes causam uma intensificação na transferência de nutrientes para o feto, aumentando o crescimento fetal.[11]
Estudos relacionaram níveis mais elevados de glicose materna a um aumento no peso ao nascer, bem como a diferentes graus de morbidade, entre eles a incidência de malformações congênitas, apoiando a hipótese de que mesmo um aumento moderado da glicose no sangue, na ausência de diabetes, influencia positivamente o crescimento fetal.[12][13]
Posteriormente, ocorreram alterações na hipótese de Pedersen: outros nutrientes além do açúcar e sua ligação ao crescimento fetal excessivo em gestações diabéticas também foram considerados, mas o papel central do hiperinsulinismo fetal e o monitoramento da glicose materna continuaram a ser ressaltados. Estudos recentes apontaram que o diabetes materno pode gerar efeitos ainda mais duradouros na saúde da criança do que se pensava anteriormente, inclusive aumentando o risco de obesidade e diabetes tipo 2.[14]
Casos históricos
[editar | editar código fonte]Diversas condições nutricionais, tanto períodos de escassez quanto de abundância, ocorreram repetidamente em diferentes sociedades e épocas. Em alguns casos, estudos epidemiológicos expuseram uma correlação entre o estado nutricional de gestantes e a saúde de seus filhos ou até netos.

A fome holandesa
[editar | editar código fonte]Como o baixo peso ao nascer está associado a um risco aumentado de doenças crônicas na vida adulta, e a nutrição materna inadequada durante a gestação pode contribuir para restrição do crescimento fetal, a subnutrição materna pode influenciar nos desfechos de saúde em longo prazo.
A Fome Holandesa de 1944, também chamada de "Inverno da Fome", durante a Segunda Guerra Mundial, serve como um estudo epidemiológico utilizado para examinar os efeitos da subnutrição materna em diferentes estágios gestacionais. Essa fome ocorreu por cerca de cinco a seis meses no oeste dos Países Baixos e envolveu uma redução significativa na disponibilidade de alimentos.[15]
A fome foi imposta a uma população previamente bem nutrida e a ração oficial para a população adulta geral diminuiu gradualmente de 1800 calorias em dezembro de 1943 para 1400 calorias em outubro de 1944 e para menos de 1000 calorias no final de novembro de 1944.[16]
Entre dezembro de 1944 e abril de 1945, a ingestão calórica caiu ainda mais para cerca de 400–800 calorias por dia.[16] Embora gestantes e lactantes tenham recebido alimentos adicionais, esses suprimentos ficaram limitados durante o auge da fome.[15]
No início de maio de 1945, a libertação dos Países Baixos restaurou o fornecimento de alimentos. A ração diária aumentou para mais de 2000 calorias em junho de 1945.[16]
O que distingue a fome holandesa como contexto de estudo é o período de tempo bem definido, a localização geográfica e o início e término abruptos da escassez em uma população previamente bem nutrida.[15]
Pesquisas relacionaram a desnutrição materna nesse período ao crescimento intrauterino restrito e a um risco aumentado de doenças crônicas na vida adulta, incluindo a doença cardíaca coronariana.[15] Essas observações são consistentes com a hipótese de Barker, que sugere que ambientes nutricionais precoces podem ter efeitos duradouros nos desfechos de saúde.
O paradoxo francês
[editar | editar código fonte]O Paradoxo francês refere-se ao aparente paradoxo de que pessoas vivendo na França há muitas gerações sofrem de baixa incidência de doença cardíaca, apesar de a cozinha francesa tradicional ser rica em ácidos graxos saturados.
Uma das explicações sugeridas para o paradoxo é o impacto potencial de melhorias nutricionais durante a gestação e os primeiros meses e anos de vida, influenciando positivamente a saúde das gerações seguintes: após a derrota na Guerra Franco-Prussiana, o governo francês introduziu um programa de nutrição para gestantes e crianças pequenas, com o objetivo de fortalecer futuras gerações de soldados. Isso pode ser uma explicação para os resultados positivos em saúde nas gerações seguintes.[17][18]
Outras pesquisas indicam a influência de fatores psicológicos e culturais na redução das mortes por doença cardíaca coronariana.[19]
Comparados a outros países, estudantes universitários na França associam menos a comida à saúde e mais ao prazer, o que pode levar a atitudes mais positivas em relação à alimentação.[19] Pesquisas preliminares sugerem que essas perspectivas francesas podem se correlacionar com menor risco de desenvolver estágios pré-clínicos de DAC. No entanto, nem todas as pesquisas apoiam essas conexões.[19]
Recomendações para gestantes
[editar | editar código fonte]Estágios da gestação
[editar | editar código fonte]A Gestação é o período de desenvolvimento embrionário do conceito até o nascimento. A gestação em humanos dura cerca de 40 semanas e é dividida em três trimestres, cada um com 3 meses.
Os estágios gestacionais, por outro lado, são baseados no desenvolvimento fisiológico fetal, incluindo: estágio germinal, estágio embrionário e estágio fetal.
Estágio germinal: vai da fecundação até cerca de 2 semanas.[20] O óvulo fecundado ou zigoto torna-se um blastocisto, onde a camada externa e a massa celular interna se diferenciam para formar, respectivamente, a placenta e o feto. A implantação ocorre neste estágio, quando o blastocisto se fixa no endométrio.
Estágio embrionário: vai de aproximadamente 2 a 8 semanas. Nesse estágio, o blastocisto desenvolve-se em um embrião, onde todas as principais estruturas humanas já estão presentes e funcionais ao final desse período.
Estágio fetal: vai da 9ª semana até o termo. Nesse período, o embrião desenvolve-se rapidamente e torna-se um feto. A gestação torna-se visível nessa fase.
-
Embrião com 8 semanas após a fertilização[21]
-
Feto com 18 semanas após a fertilização[22]
-
Feto com 38 semanas após a fertilização[23]
Peso antes da gravidez e ganho de peso gestacional
[editar | editar código fonte]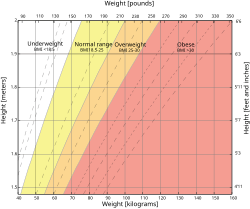
O padrão e a quantidade de ganho de peso estão intimamente associados às fases da gestação. Energia adicional é necessária durante a gravidez devido à expansão dos tecidos maternos e às reservas que dão suporte ao desenvolvimento fetal.
No primeiro trimestre (blastogênese e estágios iniciais do embrião), a mãe apresenta um ganho de peso mínimo (aproximadamente 0,5–2 kg), enquanto o embrião pesa apenas cerca de 6 gramas.
No segundo trimestre e no terceiro trimestre (estágios finais do embrião e fetal), o feto passa por rápido crescimento de peso, chegando a cerca de 3000–4000 gramas. É também nesse período que ocorre a maior parte do ganho de peso gestacional da mãe, mas a quantidade de ganho varia bastante. O total de ganho de peso depende fortemente do peso anterior à gravidez.
De modo geral, recomenda-se fortemente que as mulheres tenham peso normal ao iniciar a gestação, pois isso favorece a saúde geral dos bebês.[5] O peso corporal materno é determinado pelo Índice de massa corporal (IMC), definido como o peso em quilogramas dividido pelo quadrado da altura em metros.[24] Durante a gravidez, o peso corporal deve ser controlado dentro da faixa recomendada de ganho de peso gestacional, pois isso tem efeito positivo nos resultados da gestação. O ganho de peso deve ser progressivo e a quantidade recomendada depende do peso anterior à gravidez.
Como o ganho total depende do peso prévio, recomenda-se que mulheres abaixo do peso tenham um ganho maior para garantir bons resultados gestacionais, enquanto mulheres com sobrepeso ou obesidade tenham um ganho menor.[5]
Peso normal para mulheres
[editar | editar código fonte]
Mulheres com IMC de 18,5–24,9 são classificadas como tendo peso normal ou saudável. Esse grupo apresenta menor risco de desfechos adversos no parto.[5] Os bebês desse grupo são menos propensos a nascer com baixo peso ou com peso elevado. Recomenda-se que mulheres com peso normal antes da gravidez ganhem entre 11,5 e 16,0 kg ao longo da gestação, o que equivale a aproximadamente 0,4 kg por semana no segundo e terceiro trimestres.[5]
Para manter um ganho de peso equilibrado, a gestante deve realizar atividades físicas leves. Praticar atividades aeróbicas, como caminhada e natação, 3 a 4 vezes por semana geralmente é suficiente.[5] Atividade física vigorosa não é recomendada, pois pode causar gasto excessivo de calorias, insuficiente para sustentar o desenvolvimento fetal.
Uma dieta adequada também é essencial para um ganho de peso saudável. O ditado comum "a mulher está comendo por dois" frequentemente leva à ideia de que deve-se comer o dobro. Na realidade, apenas um pequeno aumento na ingestão calórica é necessário: cerca de 350 calorias a mais no segundo trimestre e 450 no terceiro trimestre.[5] Essas calorias extras devem vir de escolhas saudáveis, como produtos de cereal integral, frutas e vegetais, além de alternativas lácteas com baixo teor de gordura.[5]
Mulheres abaixo do peso
[editar | editar código fonte]Mulheres são classificadas como abaixo do peso se possuem IMC pré-gestacional de 18,5 ou menor.[5] Um IMC baixo antes da gravidez aumenta o risco de bebês com baixo peso ao nascer, mas esse risco pode ser equilibrado com um ganho de peso adequado entre 12,5 e 18,0 kg no total, ou cerca de 0,5 kg por semana no segundo e terceiro trimestres.[5]
Mulheres abaixo do peso geralmente têm reservas nutricionais insuficientes para sustentar a si mesmas e ao feto.[5] Embora exercício e dieta adequada sejam necessários, o equilíbrio entre ambos é fundamental. Por isso, gestantes nessa condição devem buscar orientação individualizada, adaptada ao seu caso.[5]
Mulheres com sobrepeso e obesidade
[editar | editar código fonte]Mulheres com peso elevado antes da gravidez são classificadas como com sobrepeso ou obesas, definidas como aquelas com IMC de 25 ou mais.[5] Mulheres com IMC entre 25 e 29,9 estão na categoria de sobrepeso e devem ganhar entre 7,0 e 11,5 kg no total, o que corresponde a cerca de 0,28 kg por semana no segundo e terceiro trimestres.[5] Já mulheres com IMC de 30 ou mais são consideradas obesas e devem ganhar apenas entre 5,0 e 9,0 kg no total, cerca de 0,2 kg por semana no segundo e terceiro trimestres.[5]
Dieta, exercícios ou a combinação de ambos reduzem o ganho de peso na gravidez em 20% e diminuem a pressão alta.[25] Dieta combinada com exercícios pode reduzir o risco de parto por cesariana, de ter um bebê grande ou com sérios problemas respiratórios.[25] Comparadas a mulheres sem acompanhamento ou com apenas uma sessão de rotina, aquelas que recebem orientação sobre dieta e exercícios têm menor risco de ganho excessivo de peso durante a gravidez.[25]
De modo geral, a caminhada é incentivada para gestantes dessa categoria.[5] Contudo, estimativas de necessidades energéticas não estão disponíveis.[5] Assim, recomenda-se que registrem seus níveis de atividade e ingestão. Ferramentas como o My Food Guide Servings Tracker, da Health Canada, e o EATracker disponíveis online podem auxiliar.[5] Em casos extremos, quando o IMC ultrapassa 35, recomenda-se apoio de um nutricionista registrado.[5]
Tabela Resumida
[editar | editar código fonte]A tabela a seguir resume a taxa recomendada de ganho de peso e o ganho total de peso de acordo com o Índice de Massa Corporal (IMC) pré-gestacional para gestações únicas.[26] A primeira coluna categoriza o tipo de peso corporal com base no IMC. A segunda coluna resume o ganho total de peso recomendado para cada tipo de peso corporal, e a terceira coluna apresenta o ganho de peso semanal correspondente durante o período em que o feto passa por crescimento acelerado (durante o segundo e o terceiro trimestres). Em casos extremos, a quantidade de ganho total e semanal de peso pode variar em até duas vezes, dependendo do peso da mulher antes da gravidez. Por exemplo, recomenda-se que uma mulher na categoria obesa ganhe entre 5 e 9 quilos no total, enquanto uma mulher com baixo peso precisa ganhar até 18 quilos.
| Categoria de IMC pré-gestacional | Ganho total de peso recomendado | Ganho de peso semanal
(após 12 semanas) |
|---|---|---|
| Baixo peso
IMC <18,5 |
12,5~18 kg (28~40 lb) | 0,5 kg (1,0 lb) |
| Peso saudável
IMC 18,5~24,9 |
11,5~16 kg (25~35 lb) | 0,4 kg (1,0 lb) |
| Sobrepeso
IMC 25,0~29,9 |
7,0~11,5 kg (15~25 lb) | 0,3 kg (0,6 lb) |
| Obesidade
IMC ≥ 30 |
5,0~9,0 kg (11~20 lb) | 0,2 kg (0,5 lb) |
Recomendações para Baixo e Alto Peso ao Nascer
[editar | editar código fonte]Diagnóstico
[editar | editar código fonte]
Para ter uma boa estimativa do peso ao nascer, são necessários a ultrassonografia durante a gestação e a data da última menstruação.[27] Os valores medidos por ultrassonografia são comparados com a curva de crescimento para estimar o peso fetal.[28]
O comprimento cabeça-nádega pode ser usado como a melhor medida ultrassonográfica para diagnóstico correto da idade gestacional durante o primeiro trimestre.[27] Essa correlação entre o comprimento cabeça-nádega e a idade gestacional é mais eficaz quando não há defeitos de crescimento no primeiro trimestre.[27] Se forem observados defeitos de crescimento no primeiro trimestre, a data da última menstruação torna-se importante, já que o comprimento cabeça-calcanhar se torna um indicador menos confiável da idade gestacional.[27]
Após a 20ª semana de gestação, a mãe deve visitar o médico para a medição da altura uterina, que é a distância do topo do útero até o osso púbico.[28] O comprimento medido em centímetros deve corresponder ao número de semanas de gestação.[28] Se o valor medido for maior ou menor que 2 centímetros, exames adicionais com ultrassom são necessários para confirmar os resultados.[28] Outra forma de estimar o tamanho fetal é observar o ganho de peso materno.[28] A quantidade de peso ganho pela mãe pode indicar o tamanho do feto.[28]
Baixo Peso ao Nascer
[editar | editar código fonte]
Existem duas formas de determinar pequenos para a idade gestacional (PIG). Muitos estudos concordam que bebês PIG são aqueles com peso ao nascer ou comprimento cabeça-calcanhar duas devições padrão ou mais abaixo da média da idade gestacional, com base em dados de uma população de referência.[27] Outros estudos classificam os PIG como aqueles com peso ao nascer abaixo do 10º percentil da curva de crescimento para bebês da mesma idade gestacional.[29] Isso indica que esses bebês pesam menos do que 90% dos bebês da mesma idade gestacional.
Muitos fatores, incluindo maternos, placentários e fetais, contribuem para o crescimento fetal prejudicado.[27] Entre os fatores maternos estão idade, estado nutricional, uso de álcool, tabagismo e condições médicas.[27] Perfusão útero-placentária insuficiente é um exemplo de fator placentário.[27] Anomalias cromossômicas e doenças genéticas são exemplos de fatores fetais.[27]
As complicações para o recém-nascido incluem limitações no crescimento corporal, já que o número e o tamanho das células nos tecidos é menor.[28] O bebê provavelmente não recebeu oxigênio suficiente durante a gestação, levando a baixos níveis de oxigênio.[28] Também é mais difícil manter a temperatura corporal devido ao menor fluxo sanguíneo em um corpo pequeno.[28]
Por isso, é necessário monitorar o nível de oxigênio para garantir que não fique muito baixo. Se o bebê não conseguir sugar bem, pode ser necessário utilizar sonda para alimentação.[28] Como o bebê não consegue manter a temperatura corporal adequadamente, uma incubadora aquecida ajudaria a evitar a perda de calor.[28] Há formas de ajudar a prevenir PIG. O monitoramento do crescimento fetal pode identificar o problema durante a gestação, bem antes do nascimento.[28] Buscar acompanhamento profissional e aconselhamento pode ser benéfico.
Alto peso ao nascer
[editar | editar código fonte]
Pesquisas mostram que quando os pesos ao nascer de bebês são maiores que o percentil 90 do gráfico de crescimento para bebês da mesma idade gestacional, eles são considerados grande para a idade gestacional ou GIG.[30] Isso é conhecido como macrossomia, indicando que o bebê pesa mais do que 90% dos outros na mesma idade gestacional.[30]
Muitos fatores explicam os bebês GIG, incluindo genética e suprimento excessivo de nutrientes.[30] Parece que um fator comum para bebês GIG é se a mãe tem ou não diabetes durante a gravidez.[30] Existem muitas complicações associadas a mães que dão à luz bebês GIG, e o crescimento excessivo aumenta as chances de um parto prematuro e de cesariana. Após o nascimento, o bebê está em maior risco de hipoglicemia (baixa glicose no sangue) e dificuldade para respirar.[30]
Para evitar o crescimento fetal excessivo, é importante que as mães façam consultas regulares com seu obstetra para acompanhar seu estado de saúde e detectar sinais de diabetes gestacional.[30] Para mães diabéticas, o manejo cuidadoso do diabetes durante a gestação também reduzirá o risco de dar à luz um bebê GIG.[30]
Pesquisa
[editar | editar código fonte]Desnutrição e a placenta
[editar | editar código fonte]A placenta pode se adaptar à desnutrição materna em um esforço para apoiar o desenvolvimento fetal e proteger contra exposições nutricionais adversas. Em camundongos prenhes, a subnutrição e dietas ricas em gordura demonstraram alterar tanto o tamanho quanto a estrutura da placenta, incluindo a expressão de sistemas de transporte chave.[31] Placentae de mães alimentadas com dieta rica em gordura pareceram se adaptar ao suprimento excessivo de nutrientes, enquanto placentae de mães subnutridas eram menos maduras e apresentavam transporte prejudicado.[31] Essas adaptações placentárias podem ajudar a explicar por que descendentes de gestações desnutridas apresentam crescimento alterado.[31]
Uma avaliação interseccional
[editar | editar código fonte]À medida que mais pesquisas foram produzidas para determinar a importância da saúde e nutrição pré-natal, cientistas começaram a conectar esses conceitos biológicos a ecossistemas sociais ao redor do mundo.
A nutrição pré-natal adequada só é possível se as pessoas grávidas tiverem acesso a alimentos saudáveis e acessíveis, bem como à educação para implementar uma dieta suficiente. Em muitos países de baixa renda, as mulheres frequentemente enfrentam desafios para atender às maiores demandas de micronutrientes associadas à gravidez, em grande parte devido a inadequações dietéticas persistentes.[9] Agravando esse problema, as barreiras financeiras e logísticas para avaliar indicadores bioquímicos de micronutrientes individuais resultaram em dados limitados em nível populacional sobre deficiências durante a gravidez.[9] Essa lacuna de conhecimento foi chamada de "fome oculta", refletindo tanto a escala não reconhecida do problema quanto suas potenciais consequências.
Essa falta de dados não é exclusiva de comunidades de baixa renda, mas também é evidente em países de alta renda.[9] No entanto, as informações disponíveis mostram que deficiências clínicas de micronutrientes durante a gravidez são relativamente incomuns em países de alta renda. Essa disparidade está frequentemente ligada a fatores como diversidade alimentar consistente, acesso a aconselhamento nutricional durante a gravidez, disponibilidade de alimentos fortificados e uso rotineiro de suplementos de micronutrientes no pré-natal.[9]
O ambiente intrauterino é afetado por mais do que apenas a nutrição pré-natal; depende, na verdade, da saúde geral da mãe. A saúde é definida por uma ampla gama de condições fisiológicas e genéticas, e alguns cientistas afirmam que estas também não estão imunes aos impactos das desigualdades sociais.[32] Embora a raça seja amplamente considerada uma construção social, alguns pesquisadores argumentam que os efeitos do racismo e da opressão sistêmica transformaram esse rótulo em algo mais tangível. Diferentes grupos raciais conferem vantagens e desvantagens únicas dependendo do contexto em que são analisados.[32] As desigualdades vividas por comunidades têm o potencial de ser transmitidas através das gerações, criando um ciclo de retroalimentação positiva que resulta em piores desfechos de saúde.[32] Aqueles submetidos ao racismo são mais vulneráveis à hipertensão, diabetes e acidente vascular cerebral, todos os quais impactam negativamente o ambiente intrauterino e, portanto, a saúde futura da prole.[32] Todos esses fatores representam riscos de saúde para a mãe e o feto, evidentes pelas variações no peso ao nascer discutidas acima.
Essas ideias parecem apoiar a hipótese de Barker, que afirma que o ambiente materno é essencial para o crescimento fetal adequado e para a saúde após o nascimento.[7] Outras pesquisas avaliaram os pesos ao nascer de mulheres negras nascidas nos EUA, mulheres negras nascidas na África e mulheres brancas nascidas nos EUA. Os resultados indicam um peso médio menor para mulheres negras nascidas nos EUA, em comparação com as médias mais altas e relativamente iguais de mulheres negras nascidas na África e mulheres brancas nascidas nos EUA.[32] Esses dados sugerem que existe um elemento biológico da raça, e um que pode persistir ao longo da vida, manifestando-se como doença crônica na vida adulta.[32] Quando essas crianças têm seus próprios filhos, os efeitos são transmitidos e o ciclo continua.
A interação entre esses fatores sociais, variações genéticas e variáveis ambientais, como a nutrição pré-natal, ainda apresenta muitas incógnitas que precisam ser exploradas.
Direções futuras para a pesquisa
[editar | editar código fonte]É razoável esperar maior ganho de peso em gestações múltiplas.[5] Recomendações para mulheres grávidas de gêmeos existem, mas mais pesquisas devem ser feitas para determinar com precisão o ganho de peso total, já que essas faixas são amplas.[5] Além disso, os intervalos para mulheres com baixo peso que carregam gêmeos são desconhecidos. Não há informações suficientes para recomendar limites de ganho de peso e diretrizes para mulheres grávidas de três ou mais bebês, mulheres de baixa estatura (<157 centímetros) e adolescentes grávidas.[5]
As necessidades energéticas estimadas (NEE) para mulheres com sobrepeso/obesidade também não estão disponíveis, o que torna desafiador para pessoas nessa categoria acompanhar e ajustar adequadamente suas dietas e ganho de peso.[5] Existem também ligações importantes entre nutrição e saúde mental durante a gravidez. Por exemplo, uma mulher que experimenta humor deprimido pode ter maior probabilidade de fumar, consumir álcool ou negligenciar sua dieta, todos os quais representam ameaças ao crescimento e desenvolvimento fetal (antes e depois do nascimento).[33]
As atuais recomendações de ingestão dietética de referência são geralmente baseadas em dados de indivíduos saudáveis, oferecendo percepções limitadas sobre as necessidades de mulheres grávidas, particularmente aquelas com deficiências pré-existentes.[9] Mais pesquisas são necessárias para explorar o impacto da suplementação de micronutrientes durante o período de pré-concepção e refinar recomendações dietéticas.[9] Fortalecer dados específicos da gravidez e padronizar sua interpretação será essencial para avaliar com precisão os riscos de deficiência e aprimorar as diretrizes nutricionais tanto para indivíduos quanto para populações.
Conselhos práticos para mães
[editar | editar código fonte]Manter um ganho de peso saudável e constante durante a gravidez promove a saúde geral da mãe e da criança, além de reduzir a incidência de morbidade e mortalidade pré-natal. O ganho de peso total recomendado na gravidez depende do peso corporal anterior à gestação, sendo que questões relacionadas ao peso devem ser tratadas antes da gravidez.
Como as condições durante a gestação terão efeitos de longo prazo na saúde adulta, a "moderação" deve ser considerada tanto nas recomendações dietéticas quanto nas de atividade física. Comer uma dieta equilibrada e manter atividade física compatível com as necessidades energéticas dos alimentos consumidos é o ideal para resultados saudáveis na gravidez.[34][35] Beber líquidos em quantidade suficiente, especialmente água, auxilia no aumento do volume sanguíneo durante a gravidez e previne a desidratação e a constipação.[36] Limitar o consumo de alimentos e bebidas ricos em açúcar, sódio e calorias pode ajudar gestantes a manterem um peso saudável.[35][37] Também é recomendado acompanhar as refeições regulares com um suplemento vitamínico pré-natal diário que contenha quantidade suficiente de ácido fólico e ferro.[35]
Se o feto for previsto como de baixo peso ao nascer, pode ser benéfico aumentar a ingestão calórica, o que pode ser feito acrescentando porções extras do Guia Alimentar diariamente.[35] Se o feto for previsto como de alto peso ao nascer, devem-se consumir refeições menores e mais frequentes como forma de controle de peso.[37]
Ver também
[editar | editar código fonte]Referências
- ↑ Brett, Kendra; Ferraro, Zachary; Yockell-Lelievre, Julien; Gruslin, Andrée; Adamo, Kristi (12 de setembro de 2014). «Maternal–Fetal Nutrient Transport in Pregnancy Pathologies: The Role of the Placenta». International Journal of Molecular Sciences (em inglês). 15 (9): 16153–16185. ISSN 1422-0067. PMC 4200776
 . PMID 25222554. doi:10.3390/ijms150916153
. PMID 25222554. doi:10.3390/ijms150916153
- ↑ «Parent obesity linked to delays in child development, NIH study suggest». National Institutes of Health. 3 de janeiro de 2017. Consultado em 27 de janeiro de 2017. Arquivado do original em 4 de janeiro de 2017
- ↑ De Leon, Victoria. «Weight Problems During Pregnancy and the Effect on Your Baby». Losing Pregnancy Weight. Consultado em 3 de março de 2011. Arquivado do original em 4 de março de 2011
- ↑ Catalano, P. M. (5 de março de 2010). «The impact of gestational diabetes and maternal obesity on the mother and her offspring». Journal of Developmental Origins of Health and Disease (em inglês). 1 (4): 208–215. ISSN 2040-1744. PMC 6691723
 . PMID 25141869. doi:10.1017/S2040174410000115
. PMID 25141869. doi:10.1017/S2040174410000115
- ↑ a b c d e f g h i j k l m n o p q r s t u v w «Draft Prenatal Nutrition Guidelines for Health Professionals – Maternal Weight and Weight Gain in Pregnancy». Health Canada. 2009. Consultado em 1 de dezembro de 2010. Arquivado do original em 29 de novembro de 2010
- ↑ a b Bateson, P (2001). «Fetal experience and good adult design». International Journal of Epidemiology. 30 (5): 928–934. PMID 11689495. doi:10.1093/ije/30.5.928

- ↑ a b c d e f g h i Barker, DJP (2004). «The Developmental Origins of Adult Disease»
 . Journal of the American College of Nutrition. 23 (6): 588S–595S. PMID 15640511. doi:10.1080/07315724.2004.10719428
. Journal of the American College of Nutrition. 23 (6): 588S–595S. PMID 15640511. doi:10.1080/07315724.2004.10719428
- ↑ a b c d e Byrne, CD; Phillips, DI (2000). «Fetal origins of adult disease: epidemiology and mechanisms». J Clin Pathol. 53 (11): 822–828. PMC 1731115
 . PMID 11127263. doi:10.1136/jcp.53.11.822
. PMID 11127263. doi:10.1136/jcp.53.11.822
- ↑ a b c d e f g h Gernand, Alison D.; Schulze, Kerry J.; Stewart, Christine P.; West, Keith P.; Christian, Parul (maio de 2016). «Micronutrient deficiencies in pregnancy worldwide: health effects and prevention». Nature Reviews Endocrinology (em inglês). 12 (5): 274–289. ISSN 1759-5037. PMC 4927329
 . doi:10.1038/nrendo.2016.37
. doi:10.1038/nrendo.2016.37
- ↑ Erhöhte Blutzuckerwerte bei Schwangeren gefährden das Kind
- ↑ Farmer, G.; Russell, G.; Hamilton-Nicol, D. R.; Ogenbede, H. O.; Ross, I. S.; Pearson, D. W. M.; Thom, H.; Kerridge, D. F.; Sutherland, H. W. (1988). «The influence of maternal glucose metabolism on fetal growth, development and morbidity in 917 singleton pregnancies in nondiabetic women». Diabetologia. 31 (3): 134–141. PMID 3286340. doi:10.1007/BF00276845
- ↑ Scholl, Theresa O.; Sowers, Maryfran; Chen, Xinhua; Lenders, Carine (2001). «Maternal Glucose Concentration Influences Fetal Growth, Gestation, and Pregnancy Complications». American Journal of Epidemiology. 154 (6): 514–520. PMID 11549556. doi:10.1093/aje/154.6.514

- ↑ Macfarlane CM, Tsakalakos N (1988). «The extended Pedersen hypothesis». Clin Physiol Biochem. 6 (2): 68–73. PMID 3402161
- ↑ Lindsay, Robert S. (2009). «Many HAPO Returns: Maternal Glycemia and Neonatal Adiposity: New Insights from the Hyperglycemia and Adverse Pregnancy Outcomes (HAPO) Study». Diabetes (em inglês). 58 (2): 302–303. ISSN 0012-1797. PMC 2628600
 . PMID 19171746. doi:10.2337/db08-1562
. PMID 19171746. doi:10.2337/db08-1562
- ↑ a b c d Roseboom, Tessa; Rooij, Susanne de; Painter, Rebecca (2006). «The Dutch famine and its long-term consequences for adult health». Early Human Development. 82 (8): 485–491. PMID 16876341. doi:10.1016/j.earlhumdev.2006.07.001
- ↑ a b c Hornstra, Gerard; Uauy, Ricardo; Yang, Xiaoguang (2004). The impact of maternal nutrition on the offspring. New York: Basel. ISBN 978-3-8055-7780-9
- ↑ BBC News: Health French health mystery
- ↑ Size Matters: How Height Affects the Health, Happiness, and Success of Boys
- ↑ a b c Ferrieres, J. (1 de janeiro de 2004). «The French paradox: lessons for other countries». Heart (em inglês). 90 (1): 107–111. ISSN 0007-0769. PMC 1768013
 . doi:10.1136/heart.90.1.107. Cópia arquivada em 11 de março de 2025
. doi:10.1136/heart.90.1.107. Cópia arquivada em 11 de março de 2025
- ↑ «germinal stage». Mosby's Medical Dictionary, 8th edition. Elsevier. Consultado em 2 de janeiro de 2020
- ↑ 3D Pregnancy Arquivado em 2007-09-27 no Wayback Machine (Image from gestational age of 10 weeks). Retrieved 13 December 2010. A rotatable 3D version of this photo is available here Arquivado em 2007-09-16 no Wayback Machine, and a sketch is available here Arquivado em 2007-09-27 no Wayback Machine.
- ↑ 3D Pregnancy Arquivado em 2007-09-27 no Wayback Machine (Image from gestational age of 20 weeks). Retrieved 13 December 2010. A rotatable 3D version of this photo is available here Arquivado em 2007-09-16 no Wayback Machine, and a sketch is available here Arquivado em 2007-09-27 no Wayback Machine.
- ↑ 3D Pregnancy Arquivado em 2007-09-27 no Wayback Machine (Image from gestational age of 40 weeks). Retrieved 13 December 2010. A rotatable 3D version of this photo is available here Arquivado em 2007-09-16 no Wayback Machine, and a sketch is available here Arquivado em 2007-09-27 no Wayback Machine.
- ↑ «Canadian Guidelines for Body Weight Classification in Adults». Health Canada. 2003. Consultado em 27 de novembro de 2010. Arquivado do original em 25 de março de 2010
- ↑ a b c Muktabhant, B; Lawrie, TA; Lumbiganon, P; Laopaiboon, M (15 de junho de 2015). «Diet or exercise, or both, for preventing excessive weight gain in pregnancy.». The Cochrane Database of Systematic Reviews. 2015 (6): CD007145. PMC 9428894
 . PMID 26068707. doi:10.1002/14651858.CD007145.pub3
. PMID 26068707. doi:10.1002/14651858.CD007145.pub3
- ↑ «Weight Gain During Pregnancy: Reexamining the Guidelines». Institute of Medicine. 2009. Consultado em 28 de novembro de 2010. Arquivado do original em 23 de outubro de 2009
- ↑ a b c d e f g h i Lee, PA; Chernausek, SD; et al. (2003). «International Small for Gestational Age Advisory Board Consensus Development Conference Statement: Management of Short Children Born Small for Gestational Age, April 24 – October 1, 2001». Pediatrics. 111 (6): 1253–1261. PMID 12777538. doi:10.1542/peds.111.6.1253
- ↑ a b c d e f g h i j k l "Small for Gestational Age", Lucile Packard Children's Hospital, 2010. Retrieved 9 November 2010.
- ↑ Merialdi, M; Carroli, G; et al. (2003). «Nutritional Interventions during Pregnancy for the Prevention or Treatment of Impaired Fetal Growth: An Overview of Randomized Controlled Trials» (PDF). The Journal of Nutrition. 133 (5): 1626S–1631S. PMID 12730476. doi:10.1093/jn/133.5.1626S

- ↑ a b c d e f g Children's Hospital of Wisconsin, "Large for Gestational Age", Children's Hospital and Health System, 2010. Retrieved 9 November 2010.
- ↑ a b c Connor, Kristin L; Kibschull, Mark; Matysiak-Zablocki, Elzbieta; Nguyen, Tina Tu-Thu Ngoc; Matthews, Stephen G; Lye, Stephen J; Bloise, Enrrico (1 de abril de 2020). «Maternal malnutrition impacts placental morphology and transporter expression: an origin for poor offspring growth»
 . The Journal of Nutritional Biochemistry (em inglês). 78. ISSN 0955-2863. PMID 32004932. doi:10.1016/j.jnutbio.2019.108329 Parâmetro desconhecido
. The Journal of Nutritional Biochemistry (em inglês). 78. ISSN 0955-2863. PMID 32004932. doi:10.1016/j.jnutbio.2019.108329 Parâmetro desconhecido |article-number=ignorado (ajuda) - ↑ a b c d e f Gravlee, Clarence C. (maio de 2009). «How race becomes biology: embodiment of social inequality». American Journal of Physical Anthropology. 139 (1): 47–57. ISSN 1096-8644. PMID 19226645. doi:10.1002/ajpa.20983
- ↑ </r<Lewis, A. J., Galbally, M., Gannon T., Symeonides C., (2014) Early life programming as a target for prevention of child and adolescent mental disorders: intervention and research directions. BMC Medicine: Special issue on Prevention of Mental Disorders. 12:33 doi:10.1186/1741-7015-12-33
- ↑ Larissa Hirsch, "Staying Healthy During Pregnancy", The Nemours Foundation, 2008. Retrieved 17 November 2010.
- ↑ a b c d "Prenatal Nutrition Guidelines for Health Professionals – Background on Canada's Food Guide", Health Canada, 2009. Retrieved 23 November 2010.
- ↑ Ministry of Health Promotion, "The Juicy Story on Drinks", Queen's Printer for Ontario, 2010. Retrieved 18 November 2010.
- ↑ a b Alberta clinical experts, "Prediabetes or Impaired Glucose Intolerance" Arquivado em 2010-02-02 no Wayback Machine, HealthLink Alberta, 2008. Retrieved 21 November 2010.
![Embrião com 8 semanas após a fertilização[21]](http://upload.wikimedia.org/wikipedia/commons/6/67/Color10_weeks_pregnant.jpg)
![Feto com 18 semanas após a fertilização[22]](http://upload.wikimedia.org/wikipedia/commons/5/57/Color20_weeks_pregnant.jpg)
![Feto com 38 semanas após a fertilização[23]](http://upload.wikimedia.org/wikipedia/commons/3/3b/Color40_weeks_pregnant.jpg)