Cloreto de acetila
| Cloreto de acetila Alerta sobre risco à saúde | |
|---|---|
 | |
 | |
 | |
| Nome IUPAC | Ethanoyl chloride |
| Outros nomes | Acetyl chloride |
| Identificadores | |
| Número CAS | 75-36-5 |
| Número RTECS | AO6390000 |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | CH3COCl |
| Massa molar | 78.5 g/mol[1] |
| Aparência | líquido incolor |
| Densidade | 1.11 g/ml, líquido[1] |
| Ponto de fusão | −112 °C[1] |
| Ponto de ebulição | 51 °C[1] |
| Solubilidade em água | Reage[1] |
| Viscosidade | 320 hPa (20 °C)[1] |
| Estrutura | |
| Momento dipolar | 2.45 D |
| Riscos associados | |
| Classificação UE | Flammable (F) Corrosive (C) |
| Frases R | R11, R14, R34 |
| Frases S | S1/2, S9, S16, S26, S45 |
| Ponto de fulgor | 5 °C |
| Temperatura de auto-ignição | 390 °C |
| Limites de explosividade | 7.3–19% |
| Compostos relacionados | |
| Outros aniões/ânions | Iodeto de acetila |
| cloretos de acila relacionados | Cloreto de metanoila Cloreto de propanoila Cloreto de butirila |
| Compostos relacionados | Ácido acético |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
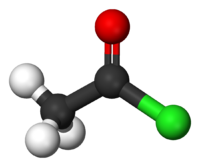
Cloreto de acetila, também conhecido como cloreto de etanoíla, é um cloreto ácido (também conhecido como cloreto de acila) derivado do ácido acético (ácido etanóico). Tem fórmula CH3COCl e pertence a classe de composto orgânicos chamados haletos de acila. A fórmula estrutural do cloreto de acetila é mostrada a direita. À temperatura e pressão ambiente, é um líquido claro e incolor. O cloreto de acetila não existe na natureza, porque em contato com água se hidrolisa em ácido acético e cloreto de hidrogênio. De fato, se manuseado ao ar livre ele produz fumaça branca própria da hidrólise com a umidade do ar. A fumaça é momentaneamente cloreto de hidrogênio gasoso o qual forma gotículas no ar com o vapor d'água.
Síntese
É quimicamente sintetizado pela reação de ácido acético com cloreto de tionila.
- CH3COO-H + O=SCl2 → CH3COCl + SO2 + H-Cl
Também pode ser sintetizado através da reação de ácido acético com tricloreto de fósforo:
- CH3COO-H + PCl3 → CH3COCl + H-Cl
Reações
O cloreto de acetila é usado como reagente para acetilação na síntese ou derivação de compostos químicos. Exemplos de reações de acetilação incluem processos de acilação tal como os de esterificação (ver abaixo) e a reação de Friedel-Crafts.
- CH3COCl + HO-CH2-CH3 → CH3-COO-CH2-CH3 + H-Cl
Frequentemente tais acilações são realizadas na presença de uma base tal qual a piridina, trietilamina, ou DMAP, as quais como catalisadores ajudam a promover a reação e como base neutralizam o HCl resultante.
Acetilação é a introdução de um grupo acetila via acilação usando um reagente tal qual o cloreto de acetila ou anidrido acético. Um grupo acetila é um grupo acila tendo a fórmula
- -C(=O)-CH3.
Para informação adicional sobre os tipos de reações químicas nas quais compostos tais como o cloreto de acetila podem participar, veja haleto de acila.
Referências
Ligações externas
- «International Chemical Safety Card 0210»
- «Acetyl Chloride-Guidechem.com»












