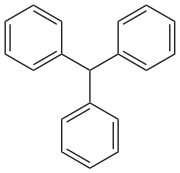
Trifenilmetán
| Trifenilmetán | |||
 | |||
 | |||
| Más nevek | trifenilmetán 1,1′,1″-metilidintriszbenzol | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 519-73-3 | ||
| PubChem | 10614 | ||
| ChemSpider | 10169 | ||
| EINECS-szám | 208-275-0 | ||
| ChEBI | 76212 | ||
| |||
| |||
| InChIKey | AAAQKTZKLRYKHR-UHFFFAOYSA-N | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C19H16 | ||
| Moláris tömeg | 244,33 g/mol | ||
| Megjelenés | színtelen, szilárd | ||
| Sűrűség | 1,014 g/cm3 | ||
| Olvadáspont | 92–94 °C | ||
| Forráspont | 359 °C | ||
| Oldhatóság (vízben) | oldhatatlan | ||
| Oldhatóság | dioxánban[1] és hexánban oldódik | ||
| Savasság (pKa) | 33 | ||
| Mágneses szuszceptibilitás | −165,6·10−6 cm3/mol | ||
| Veszélyek | |||
| R mondatok | R36 R37 R38 | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A trifenilmetán a szénhidrogének közé tartozó szerves vegyület, képlete (C6H5)3CH. Színtelen, szilárd anyag, vízben nem, de apoláris szerves oldószerekben oldódik. Számos szintetikus festékanyag, a trifenilmetán festékek alapváza, melyek közül sok pH-indikátor, némelyikük fluoreszcenciát mutat. A belőle származtatható trifenilmetilcsoportot – Ph3C – a szerves kémiában tritilcsoportnak is nevezik, pl. trifenilmetil-klorid (tritil-klorid), trifneilmetilgyök (tritilgyök).
Előállítása
Elsőként August Kekulé német kémikus és belga tanítványa, Antoine Paul Nicolas Franchimont (1844–1919) szintetizálta 1872-ben, difenil-higany (Hg(C6H5)2) és benzál-klorid (C6H5CHCl2) hevítésével.[2]
Előállítható benzolból és kloroformból Friedel–Crafts-alkilezéssel, alumínium-klorid katalizátor mellett:
- 3 C6H6 + CHCl3 → Ph3CH + 3 HCl
Egy másik lehetőség a benzolt – ugyanazon katalizátor mellett – szén-tetrakloriddal reagáltatva előállítani a tritil-klorid-alumínium-klorid adduktumot, majd ezt híg savval hidrolizálni:[3]
- 3 C6H6 + CCl4 + AlCl3 → Ph3CCl·AlCl3
- Ph3CCl·AlCl3 + HCl → Ph3CH
A benzaldehidből és foszfor-pentakloridból nyert benzilidén-kloridból kiinduló szintézisét is használják.
Savassága
A központi szénatomhoz kapcsolódó hidrogén pKa értéke 33.[4] A legtöbb más szénhidrogénhez képest jelentősen savasabb, mivel a tritil aniont stabilizálja a három benzolgyűrűre kiterjedő delokalizáció. Sztérikus okok miatt azonban a delokalizáció nem tud minden gyűrűre egyszerre kiterjedni: az egyes fenilcsoportok ugyanis a másik két gyűrűt kiszorítják a közös síkból, háromágú ventilátorra hasonló formát hozva létre; így delokalizáció csak akkor történhet, ha az anionos szénatom p-pályája párhuzamos az egyik benzolgyűrű p-pályáival. A tritil anion a látható fény tartományából erősen abszorbeál, ezért vörös színű. Ez a szín indikátorként használható a kalcium-hidriddel fenntartott vízmentes körülmények jelzésére: a hidrid vízzel reagálva kalcium-hidroxidot képez, ugyanakkor ahhoz is elég erős bázis, hogy tritil aniont hozzon létre. Amikor a hidrid teljesen elhasználódik, az oldat színtelenné válik.
Nátriumsóját tritil-kloridból is elő lehet állítani:[5]
- (C6H5)3CCl + 2 Na → (C6H5)3CNa + NaCl
A butillítium és hasonló erős bázisok elterjedése előtt gyakran használták a tritil-nátriumot nem nukleofil, erős bázisként.
Triarilmetán festékek
Trifenilmetán festék például a brómkrezolzöld:
és a nitrogént is tartalmazó malachitzöld:
Jegyzetek
- ↑ Triphenylmethane | 519-73-3
- ↑ Aug. Kekulé and A. Franchimont (1872) "Ueber das Triphenylmethan" (On triphenylmethane), Berichte der deutschen chemischen Gesellschaft, 5 : 906–908.
- ↑ J. F. Norris (1941). „Triphenylmethane”. Org. Synth.. ; Coll. Vol. 1: 548
- ↑ Ronald Breslow and William Chu (1969). „Electrochemical determinations of pKa's. Triphenylmethanes and cycloheptatriene”. Journal of the American Chemical Society 92 (7), 2165. o. DOI:10.1021/ja00710a077.
- ↑ W. B. Renfrow Jr and C. R. Hauser (1943). „Triphenylmethylsodium”. Org. Synth.. ; Coll. Vol. 2: 607
Fordítás
- Ez a szócikk részben vagy egészben a Triphenylmethane című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
 Kémiaportál • összefoglaló, színes tartalomajánló lap
Kémiaportál • összefoglaló, színes tartalomajánló lap










