Radiumnitrat
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
  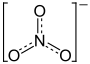 | ||||||||||
| Allgemeines | ||||||||||
| Name | Radiumnitrat | |||||||||
| Summenformel | Ra(NO3)2 | |||||||||
| Kurzbeschreibung | weißer Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 350,04 g·mol−1 | |||||||||
| Aggregatzustand | fest[1] | |||||||||
| Löslichkeit |
| |||||||||
| Gefahren- und Sicherheitshinweise | ||||||||||
 Radioaktiv | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Radiumnitrat ist eine chemische Verbindung des Radiums aus der Gruppe der Nitrate.
Gewinnung und Darstellung
Wasserfreies Radiumnitrat wird hergestellt, indem man Radiumcarbonat mit Salpetersäure umsetzt.[1]
Eigenschaften
Radiumnitrat ist ein weißer Feststoff, der gut in Wasser löslich ist. Die Löslichkeit nimmt mit steigender Konzentration an Salpetersäure ab. Durch die geringe Löslichkeit in 80%iger Salpetersäure kann man Radiumnitrat gut von den Nitraten anderer Elemente abtrennen.[1]
Einzelnachweise
- ↑ a b c d e f Kirby, H. W. and Salutsky, Murrell L. (1964) The Radiochemistry of Radium, Subcommittee on Radiochemistry, National Academy of Sciences, abgerufen am 28. Februar 2017.
- ↑ Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung. In Bezug auf weitere Gefahren wurde dieser Stoff entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.











