Oxid praseodymito-praseodymičitý
| Oxid praseodymito-praseodymičitý | |
|---|---|
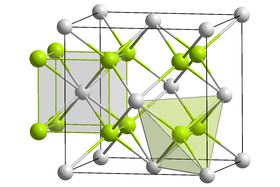 Pr3+/4+ O2− | |
| Obecné | |
| Systematický název | Oxid praseodymito-praseodymičitý |
| Německý název | Praseodym(III,IV)-oxid |
| Funkční vzorec | Pr2O3 · 4 PrO2 |
| Sumární vzorec | Pr6O11 |
| Vzhled | černá bezzápašná pevná látka[1] |
| Identifikace | |
| Registrační číslo CAS | 12037-29-5 |
| PubChem | 16211481 |
| Vlastnosti | |
| Molární hmotnost | 1 021,44 g/mol |
| Teplota tání | 2 500 °C[1] |
| Teplota varu | 4 200 °C[1] |
| Hustota | 6,5 g/cm3 (při 20 °C v pevném stavu)[1] |
| Rozpustnost ve vodě | prakticky nerozpustný ve vodě[1] |
| Bezpečnost | |
 GHS07 Varování[2] | |
| H-věty | H315, H319, H335 |
| P-věty | P261, P305+351+338[1] |
Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). Některá data mohou pocházet z datové položky. | |
Oxid praseodymito-praseodymičitý (Pr6O11) je chemická sloučenina prvků praseodymu a kyslíku, kterou lze zařadit mezi oxidy kovů.
Výskyt v přírodě
Oxid praseodymito-praseodymičitý se v přírodě nejčastěji vyskytuje jako příměs v některých minerálech, např. v bastnesitu, monazitu nebo xenotimu.[3]
Vlastnosti
Oxid praseodymito-praseodymičitý je černá pevná látka bez vůně, či zápachu, prakticky zcela nerozpustná ve vodě.[1] V základní struktuře je trojmocný praseodym zastoupen dvakrát, čtyřmocný čtyřikrát, formálně správnější by tedy byl funkční vzorec Pr2O3 · 4 PrO2. Krystalizuje v kubické krystalografické soustavě se strukturou fluoritu, kde však 1/12 kyslíkových pozic zůstává neobsazena; mřížková konstanta zde činí 5,468 Å.[4][5][6] Rozkládá se při kontaktu s vodní párou za vzniku oxidu praseodymičitého a hydroxidu praseodymitého.[7]
Za povšimnutí stojí též fakt, že existuje ještě jedna mezifáze mezi oxidem praseodymitým a oxidem praseodymičitým, s funkčním vzorcem 2 Pr2O3 · n PrO2 (kde n je libovoné číslo mezi 0 a 8), respektive sumárním vzorcem PrnO2n−2 (kde n je libovolné číslo mezi 4 a 12).[8]
Příprava/výroba
Oxid praseodymito-praseodymičitý může být získán jednoduchým spálením praseodymu za přítomnosti kyslíku.[9]
Použití
Oxid praseodymito-praseodymičitý se pro svoji sytě černou barvu používá například při barvení skla nebo keramiky.
Reference
V tomto článku byl použit překlad textu z článku Praseodym(III,IV)-oxid na německé Wikipedii.
- ↑ a b c d e f g h Záznam sloučeniny CAS 12037-29-5[nedostupný zdroj] v databázi GESTIS Institutu bezpečnosti a zdraví německé asociace pojišťovatelů, zadán dne 2. února 2013.
- ↑ a b Praseodymium(III,IV) oxide. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ SASTRI, V. S.; BUNZLI, Jean-Claude G.; RAMACHANDRA RAO, V. Modern Aspects of Rare Earths and Their Complexes. [s.l.]: Elsevier Science & Technology, 2003. Dostupné online. ISBN 978-0-44451010-5. S. 13.
- ↑ JØRGENSEN, Christian Klixbüll; RIITERSHAUS, Elfriede. Powder-diagram and Spectroscopic Studies of Mixed Oxides of Lanthanides and Quadrivalent Metals. Mat. Fys. Medd. Dan. Vid. Selsk.. 1967, roč. 15, čís. 35, s. 15. Dostupné v archivu pořízeném dne 2018-09-02.
- ↑ MCCULLOUGH, J. D. An X-Ray Study of the Rare-earth Oxide Systems: CeIV—NdIII, CrIV—PrIII, CeIV—PrIV and PrIV—NdIII. Journal of the American Chemical Society. 1950, roč. 72, čís. 3, s. 1386–1390. DOI 10.1021/ja01159a085.
- ↑ GUTH, E. Daniel; HOLDEN, J. R.; BAENZIGER, N. C.; EYRING, LeRoy. Praseodymium Oxides. II. X-Ray and Differential Thermal Analyses. Journal of the American Chemical Society. 1954, roč. 76, čís. 20, s. 5239–5242. DOI 10.1021/ja01649a088.
- ↑ BECKY L., Treu; FAHRENHOLTZ, William; O'KEEFE, Matthew; MORRIS, Eric; ALBERS, Richard. Effect of Phase on the Electrochemical and Morphological Properties of Praseodymium-Based Coatings. ECS Transactions. 2011, roč. 35, čís. 33, s. 53–66. DOI 10.1149/1.3577753.
- ↑ MASHELKAR, R. A. Solid State Chemistry: Selected Papers of C N R Rao. [s.l.]: World Scientific, 1995. ISBN 981279589-8. S. 339.
- ↑ ADACHI, Ginya; IMANAKA, Nobuhito; KANG, Zhen Chuan. Binary rare earth oxides. [s.l.]: Springer Netherlands, 2004. ISBN 978-1-40202568-6. S. 166.
Literatura
- MARTIN, R. L. Oxides of Praseodymium. Nature. 4. února 1950, roč. 165, čís. 4188, s. 202–203. DOI 10.1038/165202b0.
- WEISEMOELLER, T.; DEITER, C.; BERTRAM, F.; GEVERS, S.; GIUSSANI, A.; ZAUMSEIL, P.; SCHROEDER, T. Epitaxy of single crystalline PrO2 films on Si(111). Applied Physics Letters. 2008, roč. 93, čís. 3, s. 032905. Dostupné online [PDF]. DOI 10.1063/1.2958227. [nedostupný zdroj]
- SHAMSHI HASSAN, M.; SHAHEER AKHTAR, M.; SHIM, Kyung-Bo; YANG, O-Bong. Morphological and Electrochemical Properties of Crystalline Praseodymium Oxide Nanorods. Nanoscale Research Letters. 2010, roč. 5, čís. 4, s. 735–740. DOI 10.1007/s11671-010-9547-8.
- FERRO, Sergio. Physicochemical and Electrical Properties of Praseodymium Oxides. International Journal of Electrochemistry. 2011, roč. 2011, čís. 561204, s. 1–7. DOI 10.4061/2011/561204.
Související články
| Oxidy s prvkem v oxidačním čísle IV. | |
|---|---|
| Oxid americičitý (AmO2) • Oxid uhličitý (CO2) • Oxid ceričitý (CeO2) • Oxid chloričitý (ClO2) • Oxid chromičitý (CrO2) • Oxid dusičitý (NO2) • Oxid germaničitý (GeO2) • Oxid hafničitý (HfO2) • Oxid neptuničitý (NpO2) • Oxid olovičitý (PbO2) • Oxid manganičitý (MnO2) • Oxid molybdeničitý (MoO2) • Oxid osmičitý (OsO2) • Oxid platiničitý (PtO2) • Oxid plutoničitý (PuO2) • Oxid protaktiničitý (PaO2) • Oxid rheničitý (ReO2) • Oxid rutheničitý (RuO2) • Oxid seleničitý (SeO2) • Oxid křemičitý (SiO2) • Oxid siřičitý (SO2) • Oxid telluričitý (TeO2) • Oxid thoričitý (ThO2) • Oxid cíničitý (SnO2) • Oxid titaničitý (TiO2) • Oxid wolframičitý (WO2) • Oxid uraničitý (UO2) • Oxid vanadičitý (VO2) • Oxid zirkoničitý (ZrO2) | |
| viz též Trioxid uhlíku (CO3) • Oxid praseodymito-praseodymičitý (Pr6O11) • Oxid rhodito-platiničitý (Rh2PtO5) | |
| Anorganické soli praseodymité | |
|---|---|
| Halogenidy a pseudohalogenidy | |
| Soli kyslíkatých kyselin (neuvedeny soli | Chlorečnan praseodymitý (Pr(ClO3)3) • Chloristan praseodymitý (Pr(ClO4)3) • Bromičnan praseodymitý (Pr(BrO3)3) • Jodičnan praseodymitý (Pr(IO3)3) • Orthojodistan praseodymitý (Pr5(IO6)3) • Metajodistan praseodymitý (Pr6I4O23) • Siřičitan praseodymitý (Pr2(SO3)3) • Síran praseodymitý (Pr2(SO4)3) • Dithionan praseodymitý (Pr2(S2O3)3) • Seleničitan praseodymitý (Pr2(SeO3)3) • Selenan praseodymitý (Pr2(SeO4)3) • Dusičnan praseodymitý (Pr(NO3)3) • Fosforečnan praseodymitý (PrPO4) • Hydrogenfosforečnan praseodymitý (Pr2(HPO4)3) • Metafosforečnan praseodymitý (Pr(PO3)3) • Hydrogendifosforečnan praseodymitý (PrHP2O7) • Uhličitan praseodymitý (Pr2(CO3)3) • Wolframan praseodymitý (Pr2(WO4)3) • Vanadičnan praseodymitý (PrVO4) • Orthoboritan praseodymitý (PrBO3) |
| Soli tvořené záměnou vodíku ze sloučenin typu prvekx – vodíky | Hydrid praseodymitý (PrH3) • Hydroxid praseodymitý (Pr(OH)3) • Oxid praseodymitý (Pr2O3) • Oxid praseodymito-praseodymičitý (Pr6O11) • Oxid praseodymičitý (PrO2) • Sulfid praseodymitý (Pr2S3) • Tellurid praseodymitý (Pr2Te3) • Nitrid praseodymitý (PrN) • Fosfid praseodymitý (PrP) • Arsenid praseodymitý (PrAs) • Antimonid praseodymitý (PrSb) |







